Indice
Acido butirrico
| Acido butirrico | |
|---|---|
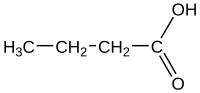 | |
 | |
| Nome IUPAC | |
| Acido butanoico | |
| Nomi alternativi | |
| Acido n-butirrico Acido etilacetico Acido propano-1-carbossilico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C4H8O2 |
| Massa molecolare (u) | 88,1 |
| Aspetto | liquido oleoso, incolore |
| Numero CAS | |
| Numero EINECS | 203-532-3 |
| PubChem | 264 |
| DrugBank | DBDB03568 |
| SMILES | CCCC(=O)O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 0,959 |
| Indice di rifrazione | 1.3991 |
| Costante di dissociazione acida (pKa) a 298,15 K | 4,82 |
| Costante di dissociazione acida a 298,15 K | 1,52 × 10⁻⁵ |
| Temperatura di ebollizione | 163,5 °C (463,5 K) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 170 °C (443 K) |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 302 - 314 |
| Consigli P | 260 - 280 - 301+312+330 - 303+340+310 - 305+351+338+310 [1] |
L'acido butirrico (dal greco βούτυρος, burro), anche denominato acido butanoico (secondo la terminologia IUPAC), è un acido carbossilico di formula CH3CH2CH2-COOH, che si trova principalmente esterificato col glicerolo in molti grassi naturali, animali e vegetali.
In forma libera si rinviene a seguito dei processi di rancidificazione (idrolisi) di detti grassi soprattutto nel burro rancido, nei formaggi stagionati (come Parmigiano Reggiano e Grana Padano), eccetera. Si forma in precisi processi di fermentazione degli zuccheri (fermentazione butirrica), e per i processi di digestione gastrica dei grassi, iniziante con l'idrolisi degli esteri gliceridi ad opera dell'acido cloridrico, si rinviene insieme agli altri acidi deboli nel vomito, oltre che nei frutti del Ginkgo biloba.
L'acido butirrico è caratterizzato dall'odore poco gradevole se presente in elevata concentrazione e dal sapore acre, con un retrogusto dolciastro (simile all'etere dietilico). In basse concentrazioni costituisce, insieme ai suoi esteri, aroma caratteristico di alcuni formaggi fermentati. L'acido butirrico è riconosciuto dai mammiferi dalle buone capacità olfattive (come i cani) in 10 ppb, e gli umani ne riconoscono concentrazioni in 10 ppm.
Il gliceride dell'acido butirrico costituisce dal 3% al 4% della massa del burro, e quando questo irrancidisce, l'acido si libera dal gliceride per idrolisi, generando il cattivo odore.
L'acido butirrico normale, detto anche acido butirrico di fermentazione, si trova anche come un estere esilico nell'olio di Heracleum giganteum e come estere octile nella Pastinaca sativa, piante della stessa famiglia; è anche stato rinvenuto nella carne viva, durante i processi di sudorazione.
Ordinariamente l'acido butirrico è un composto che si prepara dagli zuccheri o dall'amido, tramite fermentazione innescata da formaggi fermentati, con aggiunta di carbonato di calcio allo scopo di salificare altri acidi che dovessero formarsi nel processo. La fermentazione butirrica dell'amido è aiutata dall'aggiunta diretta di Bacillus subtilis.
L'acido butirrico è necessario nella preparazione di una quantità di esteri butirrati: Gli esteri dal basso peso molecolare nell'acido butirrico, come il metilbutirrato hanno in gran parte sapori e odori gradevoli, e conseguentemente trovano ampio uso nell'industria profumiera e degli aromi alimentari.
L'acido è un liquido oleoso e incolore, che solidifica a -8 °C, e bolle a 164 °C. È facilmente solubile in acqua, etanolo ed etere, ed emerge dalla sua soluzione acquosa con l'aggiunta di cloruro di calcio. Il dicromato di potassio e l'acido solforico lo ossidano in diossido di carbonio e acido acetico, mentre il basico permanganato di potassio lo ossida in diossido di carbonio. Il sale a base di calcio Ca(C4H7O2)2·H2O, è meno solubile in acqua calda che in quella fredda.
Esiste un isomero, l'acido isobutirrico, che condivide con l'acido butirrico la formula C4H8 O2, ma possiede una struttura diversa. A fronte di simili proprietà chimiche, esistono differenze tra le proprietà fisiche.
Fermentazione dei butirrati
[modifica | modifica wikitesto]Il butirrato è il prodotto finale di un processo di fermentazione unicamente eseguito da organismi anaerobici, specificamente batteri. Questo metodo di fermentazione fu scoperto da Louis Pasteur nel 1861. Tra le specie impegnate in chimica nella produzione di butirrati, enumeriamo:
- Clostridium butyricum
- Clostridium kluyveri
- Clostridium pasteurianum
- Fusobacterium nucleatum
- Butyrivibrio fibrisolvens
- Eubacterium limosum.
Il procedimento inizia con la divisione glicolitica del glucosio in due molecole di piruvato, come succede in molti organismi. Il piruvato viene poi ossidato in acetil coenzima A, usando un meccanismo unico che coinvolge un sistema enzimatico chiamato in biochimica piruvato ferredossina ossidoriduttasi. Due molecole di diossido di carbonio (CO2) e due molecole di idrogeno elementare (H2) vengono formate nella cellula e ne vengono espulse. In seguito:
- L'acetil-CoA si converte in acetoacetil-CoA; enzima responsabile: acetil-CoA-acetil transferasi.
- L'acetoacetil-CoA si converte in β-idrossibutirril-CoA; enzima responsabile: β-idrossibutirril-CoA deidrogenasi.
- β-idrossibutirril-CoA si converte in crotonil-CoA; enzima responsabile: crotonasi.
- Il crotonil-CoA si converte in butirril-CoA (CH3CH2CH2C=O-CoA); enzima responsabile: butirril-CoA-deidrogenasi.
- Un gruppo fosfato sostituisce il CoA per formare butirrilfosfato; enzima responsabile: fosfobutirrilasi.
- Il gruppo fosfato si unisce all'ADP per formare ATP e butirrato; enzima responsabile: butirrato chinasi.
L'ATP viene prodotto nella fase finale della fermentazione. Per ogni molecola di glucosio vengono prodotti 3 ATP, con una resa relativamente alta. L'equazione bilanciata per la fermentazione butirrica è:
Fermentazione dell'acetone e del butanolo
[modifica | modifica wikitesto]Diverse specie batteriche permettono la formazione di acetone e butanolo con procedimenti alternativi che partono dalla fermentazione dei butirrati.[2] Alcune di queste specie sono:
- Clostridium acetobutylicum: il produttore di acetone e butanolo più diffuso, anche nell'industria chimica
- Clostridium beijerinckii
- Clostridium tetanomorphum
- Clostridium aurantibutyricum
Questi batteri iniziano con la fermentazione dei butirrati nel modo descritto sopra, ma quando il pH scende sotto a 5, essi convertono la produzione all'acetone e al butanolo, per prevenire ulteriori cali del pH. Si formano due molecole di butanolo per ogni molecola di acetone.
I cambiamenti nelle mutazioni intervengono dopo la formazione di acetoacetil-CoA. Questo prodotto intermedio può prendere poi due vie:
- Acetoacetil CoA → acetoacetato → acetone, oppure
- Acetoacetil CoA → butirril CoA → butanale → butanolo.
Attività e funzioni dell'acido butirrico
[modifica | modifica wikitesto]Uso medico
[modifica | modifica wikitesto]L'acido butirrico è stato associato con l'abilità di inibire le funzioni dell'enzima istone deacetilasi (HDAC). Di conseguenza, favorisce uno stato acetilato degli istoni nella cellula. Gli istoni acetilati hanno un'affinità minore per il DNA rispetto agli istoni non acetilati, a causa della neutralizzazione delle interazioni di carica elettrostatica. Si pensa generalmente che i fattori di trascrizione non possano accedere a regioni dove gli istoni sono strettamente associati al DNA (come l'eterocromatina, che non è acetilata). Quindi, si pensa che l'acido butirrico aumenti l'attività trascrizionale verso quei fattori tipicamente messi a silenzio o inibiti a causa dell'attività di deacetilasi.[3]
Sperimentazione in campo oncologico ed ematologico
[modifica | modifica wikitesto]Tumore del colon-retto e malattie ematiche
[modifica | modifica wikitesto]Per questo motivo si era pensato di usarlo come agente differenziante nella terapia dei tumori, in particolare nel tumore del colon-retto, e nelle emoglobinopatie.[4] Tuttavia occorre l'assunzione di alte quantità di butirrato per poter raggiungere concentrazioni plasmatiche sufficienti perché esplichi la sua azione biologica (non inferiore ad 1 mM). In aggiunta esso è rapidamente metabolizzato per dare acetato, che entra nei mitocondri sotto forma di acetil-coenzima A. Infatti il butirrato proviene dalla fermentazione di sostanze zuccherine e dal metabolismo delle fibre vegetali. Una dieta ricca di verdure è quella più adatta per ottenere una concentrazione intestinale ottimale di acido butirrico. Esso, assieme all'aminoacido glutammina, è un normale metabolita per le cellule della mucosa del colon, che lo possono usare al posto del glucosio.[5]
Il suo derivato 4-fenilico, l'acido fenil-butirrico, come sale di sodio è più stabile ed ha un'emivita più lunga.[3][6] È stato già pubblicato uno studio pilota sugli effetti del fenilbutirrato in combinazione con un inibitore della metilazione del DNA, la 5-azacitidina, su pazienti con leucemia mieloide o sindrome mielodisplastica. Sebbene non sia risultata alcuna apparente correlazione con la risposta clinica, la combinazione dei due agenti è stata ben tollerata (irritazione nel punto di inoculazione dell'azacitidina e sonnolenza/fatica associata a fenilbutirrato di sodio) e ben il 50% dei pazienti trattati hanno avuto una remissione libera da malattia.
Tumori cerebrali
[modifica | modifica wikitesto]Un altro studio ha mostrato come il fenilbutirrato sensibilizza varie linee di cellule di glioblastoma in coltura, negative per l'oncosoppressore p53, alla radioterapia. Unito alla sua alta biodisponibilità per bocca, la sua bassa tossicità e la capacità di attraversare la barriera emato-encefalica, questo fattore ne fa un requisito cardine per la possibilità che questo composto relativamente poco tossico venga utilizzato, in un futuro molto vicino, nella terapia dei tumori cerebrali.[7]
Uso come integratore per patologie intestinali
[modifica | modifica wikitesto]Come integratore viene utilizzato per la prevenzione di malattie intestinali, per la colite, per la malattia di Crohn lieve e moderata[8], e come parte della dieta FODMAP per il trattamento della sindrome del colon irritabile.[9][4]
Altri usi non medici
[modifica | modifica wikitesto]Viene anche utilizzato dagli attivisti della Sea Shepherd contro le baleniere giapponesi. Lanciato sul ponte delle navi mattatoio esso è in grado di rovinare grandi quantità di carne di balena.[10]
È utilizzato come attrattore nella pesca sportiva, in particolare nella disciplina del carpfishing.
Note
[modifica | modifica wikitesto]- ^ scheda dell'acido butirrico su IFA-GESTIS (archiviato dall'url originale il 16 ottobre 2019).
- ^ Alais, p. 42.
- ^ a b Francesco Bottaccioli e Anna Giulia Bottaccioli, Psiconeuroendocrinoimmunologia e scienza della cura integrata. Il manuale, Edra, 31 dicembre 2016, ISBN 9788821442179.
- ^ a b (EN) Philippe R.Pouillart, Role of butyric acid and its derivatives in the treatment of colorectal cancer and hemoglobinopathies, Elsevier Inc..
- ^ (EN) Russo G.L. et al., Protective Effects of Butyric Acid in Colon Cancer, Boston, Advances in Experimental Medicine and Biology, vol 472. Springer, ISBN 978-1-4757-3230-6.
- ^ (EN) Tommaso Iannitti e Beniamino Palmieri, Clinical and Experimental Applications of Sodium Phenylbutyrate, vol. 11, n. 3, Drugs in R&D, settembre 2011, pp. 227–249, DOI:10.2165/11591280-000000000-00000.
- ^ (EN) Aline de Conti, Volodymyr Tryndyak, Igor Koturbash, Renato Heidor, Joice Kuroiwa-Trzmielina, Thomas P. Ong, Frederick A. Beland, Fernando S. Moreno, Igor P. Pogribny, The chemopreventive activity of the butyric acid prodrug tributyrin in experimental rat hepatocarcinogenesis is associated with p53 acetylation and activation of the p53 apoptotic signaling pathway, Carcinogenesis, Volume 34, Issue 8, agosto 2013.
- ^ Oral butyrate for mildly to moderately active Crohn's disease
- ^ Butyrric acid for treatment of irritable bowel syndrome Oral butyrate for mildly to moderately active Crohn's disease
- ^ Battaglia in mare tra balenieri e ambientalisti, su lastampa.it, 12 febbraio 2010.
Bibliografia
[modifica | modifica wikitesto]- Luigi Rolla, Chimica e mineralogia. Per le Scuole superiori, 29ª ed., Dante Alighieri, 1987.
- Charles Alais, Scienza del latte, 3ª ed., Tecniche Nuove, 2000, ISBN 88-481-1041-X.
- Daly K et al (2005): The importance of colonic butyrate transport to the regulation of genes associated with colonic tissue homoeostasis. Biochem. Transactions 2005: 733-735.
- Maslak P et al.: Pilot study of combination transcriptional modulation therapy with sodium phenylbutyrate and 5-azacytidine in patients with acute myeloid leukemia or myelodysplastic syndrome. Leukemia. 2006 Feb; 20(2):212-217.
- Vanhoutvin SA et al (2009): Butyrate-induced transcriptional changes in human colonic mucosa. PLoS One. 2009 Aug 25; 4(8):e6759.
- Lin J et al: A phase I dose-finding study of 5-azacytidine in combination with sodium phenylbutyrate in patients with refractory solid tumors. Clin Cancer Res. 2009 Oct 1; 15(19):6241-49.
- Lopez CA et al: Phenylbutyrate sensitizes human glioblastoma cells lacking wild-type p53 function to ionizing radiation. Int J Radiat Oncol Biol Phys. 2007 Sep 1; 69(1):214-20.
- Burkitt K, Ljungman M.: Phenylbutyrate interferes with the Fanconi anemia and BRCA pathway and sensitizes head and neck cancer cells to cisplatin. Mol Cancer. 2008 Mar 6;7:24.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su acido butirrico
Wikimedia Commons contiene immagini o altri file su acido butirrico
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) William H. Brown, butyric acid, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | LCCN (EN) sh85018405 · GND (DE) 4448004-0 · BNF (FR) cb12561820m (data) · J9U (EN, HE) 987007293671105171 |
|---|










