Indice
Cloramfenicolo
| Cloramfenicolo | |
|---|---|
 | |
 | |
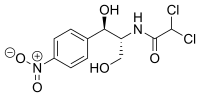
| Nome IUPAC | |
| 2,2-dicloro-N-((1R,2R)-1,3-diidrossi-1-(4-nitrofenil)propan-2-il)acetammide | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C11H12N2O5Cl2 |
| Massa molecolare (u) | 323,132 g/mol |
| Numero CAS | |
| Numero EINECS | 200-287-4 |
| Codice ATC | D06 |
| PubChem | 298 |
| DrugBank | DBDB00446 |
| SMILES | C1=CC(=CC=C1C(C(CO)NC(=O)C(Cl)Cl)O)[N+](=O)[O-] |
| Proprietà chimico-fisiche | |
| Temperatura di fusione | 149-153 |
| Dati farmacocinetici | |
| Metabolismo | Epatico |
| Emivita | 3 h |
| Escrezione | Principalmente renale |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 350 |
| Consigli P | 201 - 308+313 [1] |
Il cloramfenicolo (o cloranfenicolo), o CAF, è un antibiotico della classe degli amfenicoli, comunemente commercializzato con il nome di chemicetina.[2]
Il cloramfenicolo è utilizzato in numerose infezioni batteriche.[3] Ha azione prevalentemente batteriostatica, ma anche battericida nei confronti di Haemophilus influenzae, Pneumococco e Meningococco. Viene usato in gocce o come unguento per il trattamento delle congiuntiviti.[4] Per via orale o per iniezione endovenosa, è usato per trattare la meningite, la peste, il colera e la febbre tifoide.[3]
Nonostante il cloramfenicolo abbia discreta efficacia contro un'estesa varietà di microrganismi, per via dei seri effetti collaterali (come i danni al midollo osseo, inclusa l'anemia aplastica o la sindrome del bambino grigio nella somministrazione pediatrica), il suo impiego negli esseri umani viene limitato al trattamento d'infezioni gravi, con rischio di morte del paziente e per le quali non esista un'alternativa di pari efficacia. L'Organizzazione mondiale della sanità sostiene il suo uso nel trattamento di casi pediatrici nonostante i gravi effetti collaterali in diverse nazioni del Terzo mondo in assenza di alternative più economiche e dunque accessibili.
Il cloramfenicolo è stato scoperto nel 1947 da Ehrlich[5] che lo ha isolato a partire dal micete Streptomyces venezuelae. La sua struttura chimica è stata identificata e sintetizzata per la prima volta nel 1949.[6] Attualmente viene prodotto attraverso sintesi chimica.
Viene spesso (illegalmente) usato in apicoltura per il controllo dell'agente della peste americana Paenibacillus larvae.
Chimica
[modifica | modifica wikitesto]Il cloramfenicolo presenta all'interno della sua struttura chimica due stereocentri, con la possibile formazione di 4 diversi stereoisomeri, in cui solo il D(-) treo, presenta un'efficacia antibatterica.
Usi
[modifica | modifica wikitesto]Inizialmente il cloramfenicolo veniva utilizzato per il trattamento del tifo, ma il diffondersi di ceppi di Salmonella typhi resistente ai farmaci ha portato a una riduzione dell'impiego solo nei casi più gravi e in mancanza di un'alternativa più efficace.
Inoltre l'OMS non raccomanda più il cloramfenicolo come trattamento di prima scelta della meningite, diffuso soprattutto nei paesi a basso reddito, ma ne raccomanda l'utilizzo con cautela e solo in mancanza di alternative disponibili.[7]
Oggi il cloramfenicolo è usato principalmente come unguento per il trattamento delle congiuntiviti.[4]
Il farmaco trova impiego anche per la cura del colera, poiché colpisce i vibrioni e riduce la diarrea, risultando efficace anche nei ceppi resistenti alla tetraciclina.
L'Istituto superiore di sanità ne consiglia l'uso per il trattamento della peste[8].
Meccanismo e resistenza
[modifica | modifica wikitesto]Il cloramfenicolo agisce sui batteri, inibendo la sintesi proteica. Esso si lega alla subunità 50S ribosomiale bloccando il meccanismo di traduzione degli RNA messaggeri. Il cloramfenicolo si interpone in uno spazio della subunità 50S tra il sito A e il sito P, bloccando l'attività di peptidil-transpeptidasi, che catalizza la formazione del legame tra la catena proteica del sito P e l'aminoacido entrante nel sito A.
La resistenza al cloramfenicolo è conferita dal gene cat, il quale codifica un enzima chiamato cloramfenicolo acetiltrasferasi (in sigla CAT) che inattiva il cloramfenicolo legando con legame covalente uno o due gruppi acetili, derivati dall'acetil-S-Coenzima A, ad un gruppo idrossilico del cloramfenicolo. L'acetilazione impedisce che il cloramfenicolo si leghi al ribosoma.
Effetti collaterali
[modifica | modifica wikitesto]L'effetto collaterale più grave del trattamento con cloramfenicolo è l'anemia aplastica. Si tratta di un effetto raro ma potenzialmente fatale che si verifica settimane o mesi dopo l'interruzione del trattamento. La causa dell'insorgenza di questo effetto collaterale non è nota né prevedibile, ma potrebbe avere una componente data dalla predisposizione genetica.[3]
Il cloramfenicolo può causare la soppressione del midollo osseo; conseguenza dell'azione sui mitocondri umani.[9] La sintomatologia prevede un calo dei livelli di emoglobina, che si verifica una volta somministrata una dose cumulativa di 20 g. L'anemia è reversibile in seguito all'interruzione del farmaco e non prevede lo sviluppo dell'anemia aplastica.[10]
Il cloramfenicolo aumenta il rischio di leucemia infantile; rischio che aumenta con la durata del trattamento.[11]
La somministrazione endovenosa di cloramfenicolo è associata alla sindrome del bambino grigio.[12] Questo fenomeno si verifica nei neonati perché sono sprovvisti di enzimi epatici completamente funzionali, che non consentono il completo metabolismo del farmaco, che di conseguenza rimane non metabolizzato nell'organismo.[13] Ciò provoca diversi effetti avversi, tra cui ipotensione e cianosi. La condizione si può prevenire utilizzando il farmaco alle dosi raccomandate e monitorando i livelli ematici.[14][15]
Infine possono verificarsi reazioni di tipo allergico quali febbre, eruzioni cutanee maculari e vescicolari, angioedema, orticaria e anafilassi. Possibili sono anche le reazioni neurotossiche come mal di testa, lieve depressione, confusione mentale e delirium.[16]
Note
[modifica | modifica wikitesto]- ^ Sigma Aldrich; rev. del 26.04.2012
- ^ Cortison Chemicetina - Foglio Illustrativo, su myPersonalTrainer. URL consultato il 10 dicembre 2023.
- ^ a b c (EN) Chloramphenicol Monograph for Professionals, su Drugs.com. URL consultato il 12 agosto 2022 (archiviato il 24 giugno 2015).
- ^ a b (EN) Mark Rosenfield, Nicola Logan e Keith Edwards, Optometry: science techniques and clinical management, 2nd ed, Butterworth Heinemann Elsevier, 2009, ISBN 978-0-7506-8778-2, OCLC 317664262. URL consultato il 12 agosto 2022 (archiviato il 10 febbraio 2010).
- ^ (EN) Ehrlich J, Bartz QR, Smith RM, Joselyn AA. Chloramphenicol has been determined Chloramphenicol a New Antibiotic from Soil Actinomycetes. Science. 1947; 106: 417
- ^ (EN) Fred E. Hahn, Mechanism of Action of Antibacterial Agents, Springer Berlin Heidelberg, 1979, ISBN 978-3-642-46403-4, OCLC 840291766. URL consultato il 12 agosto 2022 (archiviato il 10 settembre 2022).
- ^ (EN) WHO Managing meningitis epidemics in Africa, su web.archive.org, 5 marzo 2016. URL consultato il 12 agosto 2022 (archiviato dall'url originale il 5 marzo 2016).
- ^ Peste - Istituto superiore di sanità, su epicentro.iss.it. URL consultato il 10 settembre 2022 (archiviato il 6 aprile 2022).
- ^ (EN) A. A. Yunis, Chloramphenicol toxicity: 25 years of research, in The American Journal of Medicine, vol. 87, 3N, 1989-09, pp. 44N–48N. URL consultato il 12 agosto 2022 (archiviato il 12 agosto 2022).
- ^ (EN) A. Morley, K. Trainor e J. Remes, Residual marrow damage: possible explanation for idiosyncrasy to chloramphenicol, in British Journal of Haematology, vol. 32, n. 4, 1976-04, pp. 525–531, DOI:10.1111/j.1365-2141.1976.tb00955.x. URL consultato il 12 agosto 2022 (archiviato il 12 agosto 2022).
- ^ (EN) X. O. Shu, Y. T. Gao e M. S. Linet, Chloramphenicol use and childhood leukaemia in Shanghai, in Lancet (London, England), vol. 2, n. 8565, 24 ottobre 1987, pp. 934–937, DOI:10.1016/s0140-6736(87)91420-6. URL consultato il 12 agosto 2022 (archiviato il 12 agosto 2022).
- ^ (EN) John McIntyre e Imti Choonara, Drug toxicity in the neonate, in Biology of the Neonate, vol. 86, n. 4, 2004, pp. 218–221, DOI:10.1159/000079656. URL consultato il 12 agosto 2022 (archiviato il 12 agosto 2022).
- ^ (EN) Víctor M. Piñeiro-Carrero e Eric O. Piñeiro, Liver, in Pediatrics, vol. 113, 4 Suppl, 2004-04, pp. 1097–1106. URL consultato il 12 agosto 2022 (archiviato il 12 agosto 2022).
- ^ (EN) H. M. Feder, Chloramphenicol: what we have learned in the last decade, in Southern Medical Journal, vol. 79, n. 9, 1986-09, pp. 1129–1134. URL consultato il 12 agosto 2022 (archiviato il 12 agosto 2022).
- ^ (EN) J. Forster, C. Hufschmidt e H. Niederhoff, [Need for the determination of chloramphenicol levels in the treatment of bacterial-purulent meningitis with chloramphenicol succinate in infants and small children], in Monatsschrift Kinderheilkunde: Organ Der Deutschen Gesellschaft Fur Kinderheilkunde, vol. 133, n. 4, 1985-04, pp. 209–213. URL consultato il 12 agosto 2022 (archiviato il 2 settembre 2022).
- ^ (EN) Chloramphenicol Sodium Succinate 1 gm Injection, USP 1 gm Vial, su dailymed.nlm.nih.gov. URL consultato il 12 agosto 2022 (archiviato il 12 agosto 2022).
Altri progetti
[modifica | modifica wikitesto] Wikizionario contiene il lemma di dizionario «cloramfenicolo»
Wikizionario contiene il lemma di dizionario «cloramfenicolo» Wikimedia Commons contiene immagini o altri file sul cloramfenicolo
Wikimedia Commons contiene immagini o altri file sul cloramfenicolo
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) chloramphenicol, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- (EN) Merck, su merck.com.
- (EN) NLM/Medline, su nlm.nih.gov.
- (EN) University of Pennsylvania, su uphs.upenn.edu.
| Controllo di autorità | Thesaurus BNCF 41222 · LCCN (EN) sh85024570 · GND (DE) 4147763-7 · J9U (EN, HE) 987007285615605171 · NDL (EN, JA) 00567045 |
|---|









