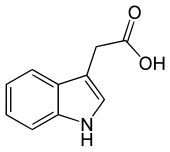
| Acido indol-3-acetico | |
|---|---|
 | |
| Nome IUPAC | |
| acido 2-(1H-indol-3-il)acetico | |
| Nomi alternativi | |
| acido indolacetico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C10H9NO2 |
| Massa molecolare (u) | 175,184 g/mol |
| Aspetto | solido bianco |
| Numero CAS | |
| Numero EINECS | 201-748-2 |
| PubChem | 802 |
| DrugBank | DBDB07950 |
| SMILES | C1=CC=C2C(=C1)C(=CN2)CC(=O)O |
| Proprietà chimico-fisiche | |
| Temperatura di fusione | 168 - 170 °C (334 - 338 °F; 441 - 443 °K) |
| Indicazioni di sicurezza | |
| Frasi H | --- |
| Consigli P | ---[1] |
L'acido indol-3-acetico (IAA) è un acido carbossilico.
Fu la prima molecola isolata del gruppo delle auxine.
Biosintesi
[modifica | modifica wikitesto]È prodotto nel meristema apicale delle gemme e nelle giovani foglie delle piante generalmente a partire dal triptofano, tuttavia alcune piante possono sintetizzarlo anche a partire da altre sostanze.
Sintesi chimica
[modifica | modifica wikitesto]Chimicamente, può essere sintetizzato facendo reagire l'indolo con acido glicolico in ambiente basico a 250 °C:[2]
Molti tipi di sintesi sono stati sviluppati dopo la sintesi originaria da indolo-3-acetonitrile.[3]
Note
[modifica | modifica wikitesto]- ^ Sigma Aldrich; rev. del 31.10.2012
- ^ Herbert E. Johnson and Donald G. Crosby, Indole-3-acetic Acid, in OrgSynth, vol. 5, 1973, p. 654.
- ^ R. Majima and T. Hoshino, Synthetische Versuche in der Indol-Gruppe, VI.: Eine neue Synthese von beta-Indolyl-alkylaminen, in Berichte der deutschen chemischen Gesellschaft, vol. 58, 1925, p. 2042, DOI:10.1002/cber.19250580917.
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su acido indol-3-acetico
Wikimedia Commons contiene immagini o altri file su acido indol-3-acetico
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) indoleacetic acid, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | LCCN (EN) sh85065729 · GND (DE) 4242054-4 · J9U (EN, HE) 987007548210705171 |
|---|









