Tiocianato
| Tiocianato | |
|---|---|
| Nome IUPAC | |
| ione tiocianato | |
| Nomi alternativi | |
| ione solfocianuro, rodanato | |
| Caratteristiche generali | |
| Formula bruta o molecolare | SCN− |
| Massa molecolare (u) | 58,08 |
| Indicazioni di sicurezza | |

Tiocianato (detto anche solfocianuro o rodanato[1]) è l'anione [SCN]−. Forma molti sali inorganici come il tiocianato di sodio e il tiocianato di potassio. In chimica organica i tiocianati sono i composti che contengono il gruppo funzionale SCN. Il tiocianato di mercurio(II) era in passato usato in pirotecnica.
Il tiocianato è analogo allo ione cianato, [OCN]−, dove uno zolfo ha sostituito l'ossigeno. Lo ione [SCN]− è uno pseudoalogenuro, perché le sue reazioni sono simili a quelle degli ioni alogenuri. Il vecchio nome rodanato (dalla parola rosa in lingua greca) deriva dal colore rosso dei suoi complessi con il ferro. Il tiocianato si forma per reazione dello zolfo elementare o del tiosolfato con il cianuro:
La seconda reazione è catalizzata dall'enzima rodanasi (una zolfo transferasi) e può essere importante nella disintossicazione dal cianuro.
Struttura, legame e chimica di coordinazione
[modifica | modifica wikitesto]La carica negativa del tiocianato è suddivisa in modo pressoché paritario tra le estremità di zolfo e azoto. Di conseguenza il tiocianato può agire da nucleofilo sia con lo zolfo che con l'azoto — è un legante ambidentato. [SCN]− può anche fungere da legante a ponte, collegando due (M−SCN−M) o anche tre metalli (come >SCN− o −SCN<). Sperimentalmente si osserva che in genere metalli che siano acidi hard tendono a legarsi con l'estremità N, mentre metalli che siano acidi soft tendono a legarsi con l'estremità S. Tuttavia sono importanti anche altri fattori cinetici e di solubilità, per cui si può osservare isomeria di legame, come ad esempio in [Co(NH3)5(NCS)]Cl2 e [Co(NH3)5(SCN)]Cl2.[2]
Nomenclatura degli isomeri di legame del tiocianato
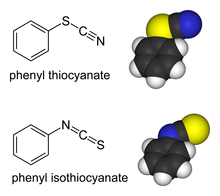
[modifica | modifica wikitesto]I derivati del tiocianato possono dar luogo a isomeri di legame, sia in molecole organiche che nei composti con metalli di transizione. Quando il gruppo organico o il metallo è attaccato allo zolfo si usa il nome tiocianati: in R−S−C≡N c'è un legame singolo S-C e un triplo legame C-N.[3] Quando il sostituente è attaccato all'azoto si usa il nome isotiocianato: in R−N=C=S ci sono due legami doppi S-C e C-N.
Reazioni
[modifica | modifica wikitesto]Lo ione tiocianato è usato in test per rivelare la presenza dei ferro(III). Aggiungendo [SCN]− ad una soluzione contenente ioni Fe3+ si forma il complesso [Fe(NCS)(H2O)5]2+, che ha un tipico colore rosso sangue.

I tiocianati organici aromatici si idrolizzano formando tiocarbammati nella sintesi di Riemschneider dei tiocarbammati:[4][5]

Note
[modifica | modifica wikitesto]- ^ In base alle attuali regole di nomenclatura chimica, la denominazione "rodanato" va evitata.
- ^ Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements, 2nd Edition, Oxford: Butterworth-Heinemann, p. 326. ISBN 0-7506-3365-4.
- ^ Guy, R. G. (1977). "Syntheses and Preparative Applications of Thiocyanates" in "Chemistry of Cyanates and Their Derivatives," vol II. Patai, S., (Editor), John Wiley, New York.
- ^ R. Riemschneider, F. Wojahn, and G. Orlick, Thiocarbamates. III.1 Aryl Thiocarbamates from Aryl Thiocyanates, in Journal of the American Chemical Society, vol. 73, n. 12, 1951, pp. 5905–5907, DOI:10.1021/ja01156a552.
- ^ Merck Index of Chemicals and Drugs, 9th ed. Organic name reactions section.
| Controllo di autorità | GND (DE) 4185249-7 · J9U (EN, HE) 987007534015405171 |
|---|













