Polianilina
La Polianilina (PANI) è un polimero conduttore della famiglia dei polimeri ad asta semi-flessibile. Anche se il composto stesso è stato scoperto più di 150 anni fa, solo a partire dai primi anni '80 la polianilina ha catturato l'intensa attenzione della comunità scientifica, grazie alla riscoperta della sua elevata conducibilità elettrica. Inserita quindi nella famiglia dei polimeri organici conduttori e semiconduttori, la polianilina ha molte caratteristiche di lavorazione interessanti ed è uno dei polimeri più studiati.[1]
Storia
[modifica | modifica wikitesto]Come descritto da Alan MacDiarmid,[2] la prima relazione definitiva sulla polianilina non apparve fino al 1862, e comprendeva un metodo elettrochimico per la determinazione di piccole quantità di anilina.[3]
Dagli inizi del XX secolo, sulla struttura del PANI sono stati pubblicati vari rapporti occasionali, e n seguito alla sua indagine di altri materiali organici altamente conduttivi, MacDiarmid ha dimostrato gli stati di conduzione di polianilina che provengono dal doping protonico della forma smeraldo della polianilina.[4] Polimeri conduttori come la polianilina rimangono di interesse notevole,[5] fornendo la possibilità di affrontare i problemi fondamentali importanti per la fisica della materia condensata, tra cui, ad esempio, la transizione metallo-isolante,[6] la Peierls Instability e la decoerenza quantica.[7]
Sintesi e proprietà
[modifica | modifica wikitesto]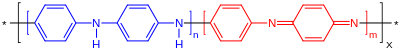
Polimerizzato dal monomero economico anilina, la polianilina può trovarsi in uno dei tre stati di ossidazione idealizzati:[8]
- leucosmeraldo – bianco/chiaro e incolore (C6H4NH)n
- smeraldo – verde per il sale smeraldino, blu per la base smeraldina ([C6H4NH]2[C6H4N]2)n
- (per) nigranilina – blu/viola (C6H4N)n
Nella figura in alto, x è uguale a metà del grado di polimerizzazione (DP). La leucosmeraldina con n = 1, m = 0 è allo stato completamente ridotto. La pernigranilina è allo stato completamente ossidato (n = 0, m = 1) con collegamenti imminici invece di legami amminici. Vari studi hanno dimostrato che la maggior parte delle forme di polianilina sono uno dei tre stati o miscele fisiche di questi componenti. Lo smeraldino (n = m = 0,5), spesso indicato come base smeraldino (EB, Emeraldine Base), è neutra, se drogata (protonata in genere) è chiamata sale smeraldino (ES), con gli atomi di azoto imminici protonati da un acido. La protonazione aiuta a delocalizzare lo stato diiminochinone-diaminobenzene altrimenti intrappolato. La EB è considerata la forma più utile di polianilina grazie alla sua elevata stabilità a temperatura ambiente e al fatto che, dopo il drogaggio con un acido, la forma di sale risultante ES della polianilina è altamente conduttrice di elettricità. La leucosmeraldina e la pernigraniline sono cattivi conduttori, anche quando drogati con un acido protico.
Il cambiamento di colore associato con la polianilina nei diversi stati di ossidazione può essere utilizzato in sensori e dispositivi elettrocromici.[9] Anche se il colore è utile, il metodo migliore per fare un sensore dalla polianilina è probabilmente quello di sfruttare i cambiamenti drastici nella conduttività elettrica tra i diversi stati di ossidazione o livelli derivanti dal doping.[10] Il trattamento della forma smeraldina con acidi aumenta la conduttività elettrica di dieci ordini di grandezza, mentre la polianilina non dopata ha una conducibilità di 6,28 × 10-9 S / m, mentre una conducibilità di 4,60 × 10-5 S / m può essere realizzata mediante drogaggio al 4% con HBr .[11] Lo stesso materiale può essere preparato per ossidazione della forma leucosmeraldina.
La polianilina è più nobile del rame e un po' meno nobile dell'argento e ciò è alla base del suo ampio utilizzo nella produzione di circuiti stampati (come finitura finale) e nella protezione contro la corrosione.[12]
Sintesi
[modifica | modifica wikitesto]Sebbene i metodi di sintesi per produrre la polianilina siano piuttosto semplici, il meccanismo di polimerizzazione è probabilmente complesso. La formazione della forma leucosmeraldina può essere descritta come segue, dove con [O] si indica un ossidante generico:[4]
- n C6H5NH2 + [O] → [C6H4NH]n + H2O
L'ossidante più comune è il persolfato di ammonio. I componenti sono ciascuno sciolti in acido cloridrico 1M (anche se possono essere usati altri acidi), e le due soluzioni (ossidante e monomero) vengono lentamente unite. La reazione è molto esotermica, ed il polimero precipita come una dispersione stabile con il particolato in scala micrometrica.
La (per) nigranilina è preparata per ossidazione della EB, utilizzando come ossidante l'acido meta-cloroperossibenzoico:[13]
- {[C6H4NH]2[C6H4N]2}n + RCO3H → [C6H4N]n + H2O + RCO2H
Lavorazione
[modifica | modifica wikitesto]La sintesi di nanostrutture a base di polianilina è comoda e senza problemi.[14]
Utilizzando procedure di polimerizzazione speciali e droganti tensioattivi, la polvere di polianilina così ottenuta può essere resa disperdibile e quindi utile per applicazioni pratiche. la sintesi di massa di nanofibre polianilina ha portato ad una forma altamente scalabile e applicabile in commercio di polianilina che è stata studiata estensivamente dalla loro scoperta nel 2002.[15]
La polianilina è tipicamente prodotta sotto forma di aggregati polimerici a catena lunga, in dispersioni di nanoparticelle stabilizzate da tensioattivi, o in dispersioni di nanofibre privo di stabilizzatore a seconda del fornitore e della via sintetica. Dispersioni di polianilina stabilizzate sono disponibili per la vendita commerciale dalla fine degli anni '90.[12]
Applicazioni
[modifica | modifica wikitesto]La polianilina e gli altri polimeri conduttori come il politiofene, il polipirrolo e il PEDOT/PSS hanno un grande potenziale di applicazioni grazie alla loro leggerezza, conduttività, flessibilità meccanica e basso costo. la polianilina è particolarmente interessante perché è relativamente poco costosa, presenta tre distinti stati di ossidazione con differenti colori e ha una risposta al doping acido/base. Quest'ultima proprietà rende la polianilina molto attraente per i sensori ai vapori di acido/base, i supercondensatori e i biosensori. I colori differenti, le cariche e le conformazioni dei molteplici stati di ossidazione rendono il materiale promettente anche per applicazioni quali attuatori, supercondensatori e sostanze elettrocromiche. Essi sono adatti per la produzione di filati elettricamente conduttivi, rivestimenti antistatici, schermature elettromagnetica ed elettrodi flessibili.[16]
Attualmente, le principali applicazioni sono la produzione di circuiti stampati (finiture finali, utilizzato in milioni di m² ogni anno), rivestimenti anti statici ed ESD, e protezione contro la corrosione.
Note
[modifica | modifica wikitesto]- ^ Okamoto, Yoshikuko and Brenner, Walter (1964) "Polymers", Ch. 7 pp. 125–158 in Organic Semiconductors, Reinhold.
- ^ (EN) Alan G. MacDiarmid, “Synthetic Metals”: A Novel Role for Organic Polymers (Nobel Lecture) [collegamento interrotto], in Angewandte Chemie International Edition, vol. 40, n. 14, 16 luglio 2001, pp. 2581-2590, DOI:10.1002/1521-3773(20010716)40:143.0.CO;2-2. URL consultato il 23 agosto 2016.
- ^ (EN) H. Letheby, XXIX.—On the production of a blue substance by the electrolysis of sulphate of aniline, in J. Chem. Soc., vol. 15, n. 0, 1º gennaio 1862, pp. 161-163, DOI:10.1039/js8621500161. URL consultato il 23 agosto 2016.
- ^ a b Jin-Chih Chiang e Alan G MacDiarmid, Proceedings of the Workshop "Synthetic Metals III" ‘Polyaniline’: Protonic acid doping of the emeraldine form to the metallic regime, in Synthetic Metals, vol. 13, n. 1, 1º gennaio 1986, pp. 193-205, DOI:10.1016/0379-6779(86)90070-6. URL consultato il 23 agosto 2016.
- ^ Alan J. Heeger, Nobel Lecture: Semiconducting and metallic polymers: The fourth generation of polymeric materials, in Reviews of Modern Physics, vol. 73, n. 3, 1º gennaio 2001, pp. 681-700, DOI:10.1103/RevModPhys.73.681. URL consultato il 23 agosto 2016.
- ^ G. Tzamalis, Applicability of the localization-interaction model to magnetoconductivity studies of polyaniline films at the metal-insulator boundary, in Physical Review B, vol. 68, n. 24, 1º gennaio 2003, DOI:10.1103/PhysRevB.68.245106. URL consultato il 23 agosto 2016.
- ^ Carlos J. Cattena, Crucial role of decoherence for electronic transport in molecular wires: Polyaniline as a case study, in Physical Review B, vol. 82, n. 14, 1º gennaio 2010, DOI:10.1103/PhysRevB.82.144201. URL consultato il 23 agosto 2016.
- ^ W. J. Feast, J. Tsibouklis e K. L. Pouwer, Symposium commemorating the 35th anniversary of PolymerSynthesis, processing and material properties of conjugated polymers, in Polymer, vol. 37, n. 22, 1º ottobre 1996, pp. 5017-5047, DOI:10.1016/0032-3861(96)00439-9. URL consultato il 23 agosto 2016.
- ^ Li-Ming Huang, Cheng-Hou Chen e Ten-Chin Wen, Development and characterization of flexible electrochromic devices based on polyaniline and poly(3,4-ethylenedioxythiophene)-poly(styrene sulfonic acid), in Electrochimica Acta, vol. 51, n. 26, 15 agosto 2006, pp. 5858-5863, DOI:10.1016/j.electacta.2006.03.031. URL consultato il 23 agosto 2016.
- ^ (EN) Shabnam Virji, Jiaxing Huang e Richard B. Kaner, Polyaniline Nanofiber Gas Sensors: Examination of Response Mechanisms, in Nano Letters, vol. 4, n. 3, 19 febbraio 2004, pp. 491-496, DOI:10.1021/nl035122e. URL consultato il 23 agosto 2016.
- ^ Hammo, Shamil M. (2012).
- ^ a b (EN) Bernhard Wessling, New Insight into Organic Metal Polyaniline Morphology and Structure, in Polymers, vol. 2, n. 4, 17 dicembre 2010, pp. 786-798, DOI:10.3390/polym2040786. URL consultato il 23 agosto 2016.
- ^ Sapurina, I. Yu. and Shishov, M. A. (2012) "Oxidative Polymerization of Aniline: Molecular Synthesis of Polyaniline and the Formation of Supramolecular Structures", in New Polymers for Special Applications, Ailton De Souza Gomes (Ed.), ISBN 978-953-51-0744-6, InTech, doi:10.5772/48758.
- ^ (EN) Gordana Ćirić-Marjanović, Polyaniline Nanostructures, in Nanostructured Conductive Polymers, John Wiley & Sons, Ltd, 1º gennaio 2010, pp. 19-98, DOI:10.1002/9780470661338.ch2, ISBN 9780470661338. URL consultato il 23 agosto 2016.
- ^ Jiaxing Huang, Shabnam Virji e Bruce H. Weiller, Polyaniline Nanofibers: Facile Synthesis and Chemical Sensors, in Journal of the American Chemical Society, vol. 125, n. 2, 1º gennaio 2003, pp. 314-315, DOI:10.1021/ja028371y. URL consultato il 23 agosto 2016.
- ^ Karsten Fehse, Gregor Schwartz e Karsten Walzer, Combination of a polyaniline anode and doped charge transport layers for high-efficiency organic light emitting diodes, in Journal of Applied Physics, vol. 101, n. 12, 15 giugno 2007, p. 124509, DOI:10.1063/1.2748864. URL consultato il 23 agosto 2016 (archiviato dall'url originale il 26 agosto 2016).
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su Polianilina
Wikimedia Commons contiene immagini o altri file su Polianilina
| Controllo di autorità | LCCN (EN) sh2014002578 · J9U (EN, HE) 987007405887705171 |
|---|








