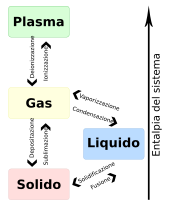
Il punto triplo è un particolare stato termodinamico determinato dai valori di temperatura e pressione in cui coesistono, in condizioni di equilibrio, tre fasi di aggregazione di una sostanza:[1] nel caso più comune, quelle solida, liquida e aeriforme.
Tuttavia molte sostanze, tra le quali l'acqua e l'anidride carbonica, hanno più di una fase solida (polimorfi), cosicché i loro diagrammi di fase presentano più punti tripli solido-solido-liquido o solido-solido-solido. I valori di temperatura e pressione che identificano i punti tripli dipendono solamente dalla sostanza in esame e, nel caso dei punti solido-liquido-aeriforme, possono essere determinati con notevole precisione grazie alla grande diversità di comportamento delle tre fasi coinvolte. Il punto triplo di varie sostanze è dunque utile per la taratura di strumenti di misura, utilizzando dispositivi metrologici chiamati "celle a punto triplo" contenenti la sostanza richiesta. La temperatura di quello dell'acqua è utilizzata per la definizione della scala kelvin. La dipendenza del punto triplo dalla composizione chimica richiede però che le sostanze campione abbiano un elevatissimo grado di purezza.
Punti tripli di alcune sostanze
[modifica | modifica wikitesto]Nella tabella seguente sono indicati i valori dei punti tripli di alcune sostanze comuni. Dove non indicato diversamente, i valori sono stati misurati dal National Bureau of Standards.[2]
| Sostanza | T (K) | P (Atm)[3] |
|---|---|---|
| Acetilene | 192,4 | 1,1843 |
| Acido cloridrico | 158,96 | 0,1372 |
| Acido formico | 281,40 | 0,0217 |
| Acqua | 273,16 | 6 × 10−3 |
| Ammoniaca | 195,40 | 0,06 |
| Anidride carbonica | 216,55 | 5,1024 |
| Anidride solforosa | 197,69 | 0,0165 |
| Argon | 83,81 | 0,68 |
| Azoto | 63,18 | 0,1244 |
| Butano | 134,6 | 7 × 10−6 |
| Carbonio (grafite) | 4765 | 99,9951 |
| Cloroformio | 175,43 | 8,586 × 10−3 |
| Deuterio | 18,63 | 0,1688 |
| Elio-4 (punto lambda) | 2,19 | 0,0503 |
| Esafluoroetano | 173,08 | 0,2625 |
| Esafluoruro di uranio | 337,17 | 1,4972 |
| Etano | 89,89 | 8 × 10−6 |
| Etanolo | 150 | 4,3 × 10−9 |
| Etilene | 104,0 | 1,184 × 10−3 |
| Idrogeno | 13,84 | 0,0695 |
| Iodio[4] | 386,65 | 0,1191 |
| Isobutano | 113,55 | 1,9481 × 10−7 |
| Mercurio | 234,2 | 1,65 × 10−9 |
| Metano | 90,68 | 0,1155 |
| Monossido di azoto | 109,50 | 0,2163 |
| Monossido di carbonio | 68,10 | 0,1517 |
| Neon | 24,57 | 0,4264 |
| Ossido di diazoto | 182,34 | 0,867 |
| Ossigeno | 54,36 | 1,5 × 10−3 |
| Palladio | 1825 | 3,5 × 10−5 |
| Platino | 2045 | 2,0 × 10−6 |
| Titanio | 1941 | 5,3 × 10−5 |
| Xeno | 161,3 | 0,8043 |
| Zinco | 692,65 | 6,42 × 10−4 |
Note
[modifica | modifica wikitesto]- ^ (EN) IUPAC Gold Book, "triple point" Archiviato il 1º giugno 2013 in Internet Archive.
- ^ Yunus A. Cengel, Robert H. Turner. Fundamentals of thermal-fluid sciences. McGraw-Hill, 2004, p. 78. ISBN 0072976756
- ^ 101,325 kPa sono pari a 1 atm.
- ^ Walas, S.M., Chemical Process Equipment - Selection and Design. Elsevier, 1990, p. 639.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file sul punto triplo
Wikimedia Commons contiene immagini o altri file sul punto triplo
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) triple point, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.