Azoturo di litio
Vai alla navigazione
Vai alla ricerca
| Azoturo di litio | |
|---|---|
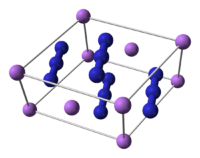 | |
| Nome IUPAC | |
| azoturo di litio | |
| Nomi alternativi | |
| litio azide azotidrato di litio | |
| Caratteristiche generali | |
| Formula bruta o molecolare | LiN3 |
| Numero CAS | |
| Numero EINECS | 243-177-1 |
| PubChem | 88163 e 4176279 |
| SMILES | [Li+].[N-]=[N+]=[N-] |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
L'azoturo di litio è il sale di litio dell'acido azotidrico.
È un composto chimico instabile e tossico, se riscaldato si decompone violentemente in azoto e litio.
Sintesi
[modifica | modifica wikitesto]Si può ottenere nitruro di litio in una reazione di doppio scambio fra:
azoturo di sodio e nitrato di litio:
NaN3 + LiNO3 → LiN3 + NaNO3
azoturo di sodio e solfato di litio:[1]
NaN3 + Li2SO4 → LiN3 + Na2SO4[2]
acetato di litio e azoturo di piombo:
2CH3COOLi + Pb(N3)2 → Pb(CH3COOH)2 + 2LiN3[senza fonte]
Note
[modifica | modifica wikitesto]- ^ Si sciolgono in 7 ml di acqua distillata 1,3 g di azoturo di sodio ed 1,41 g di solfato di litio monoidrato (riscaldando moderatamente) e si ottiene un precipitato bianco di solfato di sodio e nitruro di litio. Si aggiungono quindi 35 ml di etanolo al 96% a si mischia il tutto. Il nitruro di litio si troverà disciolto nell'etanolo. Basta filtrare il tutto, rimuovere il solfato di sodio ed essiccare la miscela di etanolo ad 80 °C.
- ^ λ » LambdaSyn – Darstellung von Lithiumazid
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su Azoturo di litio
Wikimedia Commons contiene immagini o altri file su Azoturo di litio








