Indice
Assone
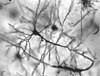
Struttura tipica di un neurone
L'assone o neurite (in generale, anche i dendriti sono classificabili come neuriti) è un conduttore di impulsi in direzione centrifuga rispetto al corpo cellulare. Ogni neurone ha unicamente un assone. Esso si origina a partire dal soma cellulare attraverso una particolare struttura anatomica che prende il nome di "cono di emergenza"; questo nome deriva dal fatto che questa struttura ha forma di tronco di cono con la base rivolta verso il "soma" cellulare e l'apice tronco che continua nell'assone. L'assone, solitamente, non presenta diramazioni nella sua porzione prossimale, mentre, nella sua porzione distale, si dirama assumendo l'aspetto della "chioma di un albero".
Anatomia
[modifica | modifica wikitesto]Nel regno animale, a seconda dello stato evolutivo, esistono due tipologie di trasmissione dell'impulso nervoso tra due cellule attigue:
- Una trasmissione puramente elettrica, in cui l'assone è a contatto diretto con le strutture del neurone "bersaglio" e avviene una depolarizzazione "per contatto" (tipica degli invertebrati).
- Una trasmissione chimica, in cui due neuroni attigui comunicano attraverso il rilascio di sostanze chimiche, che prendono il nome di "mediatori" (ad esempio acetilcolina o adrenalina); a seconda del mediatore che le fibre utilizzano per "comunicare" esse vengono classificate in modi differenti.
Le diramazioni assoniche terminali finiscono con una struttura dilatata, detta a "bottoncino", che prende il nome di sinapsi. La sinapsi viene divisa in uno spazio presinaptico (la vescicola) e uno postsinaptico (lo spazio compreso tra la vescicola e la membrana nel neurone successivo). La sinapsi contiene solo i mediatori chimici e i mitocondri necessari alla produzione energetica; la sintesi dei mediatori avviene nel soma cellulare e viene trasportato alla sinapsi attraverso il "flusso assonico". Le sinapsi possono entrare in contatto sia con il soma sia con i dendriti di altre cellule nervose.
L'assone si comporta come un conduttore elettrico; infatti grazie alla presenza di alcuni ioni come sodio, cloro, calcio e potassio, viene creato un flusso ionico che genera una corrente elettrica.
Quando arriva un impulso elettrico, questo percorre l'assone. A livello delle sinapsi la depolarizzazione determinata dalla corrente determina l'apertura di canali per il calcio. Questo determina il rilascio di una sostanza chimica detta neurotrasmettitore (come l'acetilcolina, l'acido aminoglutammico, GABA, o altri) che, legandosi a specifici recettori, permette il passaggio dell'impulso elettrico da un neurone all'altro. L'assone quindi rappresenta l'output del neurone che rilascia un impulso elettrico e allo stesso tempo l'input per i neuroni riceventi.
Il singolo assone ha un diametro microscopico di pochi micrometri, ma la sua lunghezza può raggiungere lunghezze macroscopiche. Gli assoni più lunghi del corpo umano sono quelli che costituiscono il nervo sciatico che dalla base del midollo spinale raggiungono l'alluce dei piedi e possono raggiungere lunghezze superiori al metro.
Trasporto assonale
[modifica | modifica wikitesto]L'assoplasma è l'equivalente del citoplasma cellulare. I microtubuli si formano nell'assoplasma del collicolo assonico. Sono disposti lungo l'assone, in sezioni sovrapposte, e puntano tutti nella stessa direzione, cioè verso i terminali degli assoni.[1] Studi sull'assoplasma hanno consentito di visualizzare il movimento di vescicole di tutte le dimensioni lungo i filamenti del citoscheletro, in entrambe le direzioni, tra l'assone, i suoi terminali e il corpo cellulare.
Il trasporto anterogrado in uscita dal corpo cellulare lungo l'assone, trasporta i mitocondri e le proteine di membrana necessarie per la crescita fino al terminale assonale. Il trasporto retrogrado trasporta materiali di scarto dal terminale assonico al corpo cellulare.[2] Il trasporto in uscita avviene grazie alle proteine dette chinesine quello in entrata dalle dineine.[2] Esistono molte forme di chinesina e dineina e si pensa che ciascuna di esse abbia un carico diverso.[1]
Mielinizzazione
[modifica | modifica wikitesto]Nei vertebrati gli assoni possono essere rivestiti da una guaina mielinica, formando una fibra nervosa. La guaina mielinica è uno strato isolante costituito da due tipi di cellule gliali: le cellule di Schwann per gli assoni periferici e gli oligodendrociti per il sistema nervoso centrale.
Le fibre nervose possono quindi essere:
- amieliniche, se gli assoni sono solamente contenuti in una nicchia delle cellule di Schwann, prive di isolante interagiscono con le molecole dell'ambiente circostante.
- mieliniche, se le cellule mieliniche si avvolgono più volte attorno all'assone, formando una fila di manicotti, che schermano la fibra dalla corrente ionica. Lungo le fibre mieliniche, la guaina mielinica presenta delle interruzioni, i nodi di Ranvier, che permettono una conduzione del segnale elettrico più rapida, detta "conduzione saltatoria".
Le cellule di Schwann mielinizzano un singolo assone. Un oligodendrocita può mielinizzare fino a 50 assoni.[3]
Nodi di Ranvier
[modifica | modifica wikitesto]
I nodi di Ranvier sono brevi segmenti non mielinizzati che si trovano intervallati tra i segmenti della guaina mielinica dell'assone. Nel nodo di Ranvier, l'assone ha un diametro ridotto.[4] I nodi sono aree in cui è possibile generare potenziali di azione. Le correnti elettriche prodotte in ciascun nodo di Ranvier sono condotte con sul nodo successivo, dove generano un altro potenziale di azione. Quindi, in un assone mielinizzato, i potenziali d'azione saltano da un nodo all'altro, evitando i segmenti mielinizzati in mezzo, con una velocità di propagazione più veloce rispetto agli assoni non mielinizzati più veloci.
Terminale assonale
[modifica | modifica wikitesto]Un assone può dividersi in molti rami chiamati telodendri. Alla fine di ogni telodendro c'è un terminale assonale (o bottone terminale). Nei terminali sono presenti delle vescicole sinaptiche che contengono il neurotrasmettitore che verrà rilasciato alla sinapsi. Sono possibili più connessioni sinaptiche con altri neuroni, e volte l'assone di un neurone può agire sui dendriti dello stesso neurone.
Potenziale d'azione
[modifica | modifica wikitesto]
La maggior parte degli assoni trasmette segnali sotto forma di potenziali d'azione, che sono impulsi elettrochimici che viaggiano rapidamente lungo l'assone, dal corpo cellulare al punto in cui l'assone effettua il contatto sinaptico con la cellula bersaglio. Il potenziale d'azione è "tutto o niente", ovvero che ha la stessa dimensione e forma. Questa caratteristica consente di trasmettere i potenziali da un'estremità all'altra mantenendo intensità costante. Esistono, tuttavia, alcuni tipi di neuroni con assoni corti che trasmettono segnali elettrochimici graduati, di ampiezza variabile.
Quando un potenziale d'azione raggiunge un terminale presinaptico, attiva il processo di trasmissione sinaptica. Il primo passo è l'apertura rapida dei canali ionici del calcio nella membrana dell'assone, che consentono agli ioni calcio di fluire verso l'interno. Il conseguente aumento della concentrazione di calcio intracellulare causa la fusione delle vescicole sinaptiche contenenti il neurotrasmettitore con la membrana dell'assone e lo svuotamento del loro contenuto nello spazio extracellulare. Il neurotrasmettitore viene rilasciato attraverso esocitosi, e diffonde sui recettori situati sulla membrana della cellula bersaglio. Il neurotrasmettitore si lega ai recettori e li attiva. A seconda del tipo di recettori attivati, l'effetto sulla cellula bersaglio può essere quello di eccitazione o inibizione. L'intera sequenza di eventi si svolge in meno di un millesimo di secondo. Infine all'interno del terminale presinaptico, viene posizionata una nuova serie di vescicole vicino alla membrana, pronta per essere rilasciata al successivo potenziale d'azione.[5]
Oltre a propagare i potenziali d'azione, l'assone è in grado di amplificarli, il che assicura la propagazione dei potenziali d'azione sequenziali verso il terminale assonale. In termini di meccanismi molecolari, ciò avviene perché i canali del sodio voltaggio-dipendenti negli assoni possiedono una soglia più bassa e un periodo refrattario più breve in risposta agli impulsi a breve termine.[6]
Sviluppo e crescita
[modifica | modifica wikitesto]Sviluppo
[modifica | modifica wikitesto]Lo sviluppo dell'assone è uno dei principali stadi dello sviluppo complessivo del sistema nervoso.[7] Studi condotti su neuroni ippocampali suggeriscono che i neuroni producano dei neuriti multipli, ma che solo uno di essi sia destinato a diventare l'assone.[8] Non è chiaro se la differenziazione degli assoni preceda l'allungamento degli assoni o viceversa, anche se gli studi recenti propendono per l'ultima spiegazione.[9] Se un assone non completamente sviluppato viene reciso, altri neuriti possono trasformarsi in assone, ma ciò si verifica solo quando l'assone viene tagliato almeno 10 µm più corto rispetto agli altri neuriti. Dopo l'incisione, il neurita più lungo diventerà il futuro assone e tutti gli altri neuriti, incluso l'assone originale, si trasformeranno in dendriti.[10] Agire dall'esterno su un neurite, facendolo allungare, lo farà diventare un assone.[11] Tuttavia, lo sviluppo assonale si ottiene attraverso una complessa interazione tra segnalazione extracellulare, segnalazione intracellulare e dinamica citoscheletrica.
Crescita
[modifica | modifica wikitesto]Gli assoni in crescita si muovono attraverso il cono di crescita nell'ambiente circostante. Il cono di crescita si estende tramite il lamellipodio, che contiene sporgenze dette filopodi, attraverso i quali l'intero processo aderisce alle superfici ed esplora l'ambiente. L'actina svolge un ruolo importante nella mobilità assonale. Ambienti con alte concentrazioni di molecole di adesione cellulare (CAM) creano un ambiente ideale per la crescita dell'assone. Esempi di CAM specifici per sistemi neurali comprendono N-CAM, la glicoproteina TAG-1,[12] e le MAG, che fanno parte della superfamiglia delle immunoglobuline. Un altro insieme di molecole chiamate molecole di adesione della matrice extracellulare forniscono un substrato ideale affinché gli assoni crescano. Esempi di queste molecole includono laminina, fibronectina, tenascina e perlecano. Le cellule guida, cioè neuroni non maturi, aiutano nella crescita degli assoni neuronali. Se gli assoni di un neurone sono danneggiati, si possono rigenerare fino a quando il soma (il corpo cellulare di un neurone) non viene a sua volta danneggiato. Gli assoni danneggiati possono ricostituire le connessioni sinaptiche con altri neuroni con l'aiuto di cellule guida. Questo processo è noto come neurorigenerazione.[13]
Il Nogo-A è una componente inibitoria della crescita dei neuriti presente nelle membrane mieliniche del sistema nervoso centrale. Ha un ruolo cruciale nel limitare la rigenerazione assonale nel sistema nervoso centrale dei mammiferi adulti. In studi recenti, se il Nogo-A è bloccato e neutralizzato, è possibile indurre una rigenerazione assonale a lunga distanza che porta al miglioramento del recupero funzionale nei ratti e nel midollo spinale del topo. Questo esperimento non è stato ancora fatto sugli umani.[14] Uno studio recente ha evidenziato che i macrofagi attivati attraverso una specifica via infiammatoria dal recettore Dectin-1 sono in grado di promuovere il recupero degli assoni, causando però neurotossicità.
Classificazione
[modifica | modifica wikitesto]Gli assoni dei neuroni nel sistema nervoso periferico umano possono essere classificati in base alle loro caratteristiche fisiche e alle proprietà di conduzione del segnale. Gli assoni sono noti per avere spessori diversi (da 0,1 a 20 µm)[15] e si pensava che queste differenze fossero correlate alla velocità con cui un potenziale d'azione può viaggiare lungo l'assone - la sua velocità di conduttanza. Erlanger e Gasser hanno dimostrato questa ipotesi e identificato diversi tipi di fibre nervose, stabilendo una relazione tra il diametro dell'assone e la sua velocità di conduzione nervosa. Pubblicarono le loro scoperte nel 1941 dando la prima classificazione degli assoni.
Gli assoni sono classificati in due sistemi. Il primo introdotto da Erlanger e Gasser, raggruppava le fibre in tre gruppi principali usando le lettere A, B e C. Questi gruppi, comprendono sia le fibre sensoriali (afferenti) che le fibre motorie (efferenti). Il gruppo A è suddiviso in fibre alfa, beta, gamma e delta (Aα, Aβ, Aγ e Aδ). I motoneuroni delle fibre motorie, sono i neuroni motori inferiori - alfa motoneurone, beta motoneurone e motoneurone gamma con le fibre nervose Aα, AC e Aγ rispettivamente.
Successive scoperte di altri ricercatori hanno identificato due gruppi di fibre Aa che sono fibre motorie. Poi è stato introdotto in un sistema che includeva solo fibre sensoriali (anche se alcuni di questi sono nervi misti). Questo sistema (classificazione di Lloyd-Hunt) utilizza i numeri romani, e comprende il Tipo Ia, Tipo Ib, Tipo II, Tipo III e Tipo IV.
Fibre motorie
[modifica | modifica wikitesto]I motoneuroni inferiori hanno due tipi di fibre:
| Tipo | Classificazione Erlanger-Gasser | Diametro
(μm) |
mielina | Velocità di conduzione (m/s) | Fibre muscolari associate |
|---|---|---|---|---|---|
| α | Aα | 13-20 | si | 80-120 | Fibre muscolari extrafusali |
| γ | Aγ | 5-8 | si | 4-24[16][17] | Fibre muscolari intrafusali |
Fibre sensoriali
[modifica | modifica wikitesto]Diversi recettori sensoriali innervano diversi tipi di fibre nervose, così distinte in base alla classificazione di Lloyd-Hunt: Ia, Ib, II, III e IV. I propriocettori sono innervati dalle fibre sensoriali di tipo Ia, Ib e II, i meccanocettori da fibre sensoriali di tipo II e III, i nocicettori e i termocettori da fibre sensoriali di tipo III e IV.
| Tipo | Classificazione Erlanger-Gasser | Diametro
(μm) |
mielina | Velocità di conduzione (m/s) | Recettori sensoriali associati | Propriorecettori | Meccanocettori | Nocicettori e
termocettori |
|---|---|---|---|---|---|---|---|---|
| Ia | Aα | 13-20 | si | 80-120 | Recettori primari del fuso neuromuscolare | ✔ | ||
| Ib | Aα | 13-20 | si | 80-120 | Organo tendineo del Golgi | |||
| II | Aβ | 6-12 | si | 33-75 |
|
✔ | ||
| III | Aδ | 1-5 | poca | 3-30 |
|
✔ | ||
| IV | C | 0,2-1,5 | no | 0,5-2 |
|
Fibre autonomiche
[modifica | modifica wikitesto]Il sistema nervoso autonomo ha due tipi di fibre periferiche:
| Tipo | Classificazione Erlanger-Gasser | Diametro
(μm) |
Mielina[18] | Velocità di conduzione (m/s) |
|---|---|---|---|---|
| Fibre pregangliari | B | 1-5 | si | 3–15 |
| Fibre postgangliari | C | 0.2–1.5 | no | 0.5–2.0 |
Modelli fisici di descrizione di un assone
[modifica | modifica wikitesto]A partire dai lavori pionieristici di Cole, Huxley, Curtis e Hodgkin si è provato a descrivere gli assoni in termini di circuiti elettrici, rappresentando in termini di impedenze le caratteristiche elettriche delle cellule. Numerosi sono i modelli proposti. Quelli più studiati e conosciuti sono il modello a cavo e il modello a linea di trasmissione
Patologia
[modifica | modifica wikitesto]In ordine di gravità, la lesione a un nervo può essere descritta come neuroaprassia, assonotmesi o neurotmesi.
La disfunzione degli assoni del sistema nervoso è una delle cause di molti disturbi neurologici ereditari che colpiscono sia i neuroni periferici che i neuroni centrali.[5]
La demielinizzazione degli assoni provoca la maggior parte dei sintomi neurologici riscontrati nella sclerosi multipla.
La dissielinizzazione è la formazione anormale della guaina mielinica, implicata in diverse leucodistrofie e anche nella schizofrenia.[19][20][21]
Una lesione cerebrale traumatica può causare danni alle vie nervose danneggiando gli assoni, e una condizione nota come danno assonale diffuso, che può portare a uno stato vegetativo persistente.[22] La commozione cerebrale è considerata una forma lieve di danno assonale diffuso.[23].
Storia
[modifica | modifica wikitesto]L'anatomista tedesco Otto Friedrich Karl Deiters è lo scopritore degli assoni e il primo a distinguerli dai dendriti.[5] Lo svizzero Rüdolf Albert von Kölliker e il tedesco Robert Remak furono i primi a identificare e caratterizzare il segmento iniziale degli assoni. Kölliker diede il nome all'assone nel 1896.[24] Alan Hodgkin e Andrew Huxley studiarono l'assone gigante di calamaro (1939) e nel 1952 ottennero un'analisi quantitativa completa della base ionica del potenziale d'azione, portando alla formulazione dell modello di Hodgkin - Huxley, che valse ad entrambi il Premio Nobel nel 1963. Le formule che descrivono la conduttanza assonale furono estese ai vertebrati grazie alle equazioni di Frankenhaeuser-Huxley. Il primo a descrivere i nodi assonali fu Louis-Antoine Ranvier, che per questo motivo sono comunemente chiamati nodi di Ranvier. Santiago Ramón y Cajal, un anatomista spagnolo, propose che gli assoni fossero i componenti in uscita dei neuroni, descrivendone la funzionalità.[5] Joseph Erlanger e Herbert Gasser svilupparono il sistema di classificazione delle fibre nervose periferiche, basato sulla velocità di conduzione assonale, sulla mielinizzazione, sulla dimensione delle fibre ecc. La comprensione delle basi biochimiche per la propagazione del potenziale d'azione è ulteriormente progredita e include molti dettagli sui singoli canali ionici.
Altri animali
[modifica | modifica wikitesto]Gli assoni negli invertebrati sono stati ampiamente studiati. Il calamaro atlantico, usato come organismo modello, ha l'assone più lungo conosciuto.[25] Il calamaro gigante ha il più grande assone conosciuto. Le sue dimensioni variano da un millimetro a mezzo millimetro di diametro. La velocità di conduzione più veloce registrata è di 210 m/s e si trova negli assoni di alcuni gamberetti pelagici,[26] con un range usuale compreso tra 90 e 200 m/s[27] (cfr. 100–120 m/s per l'assone vertebrato mielinizzato più veloce).
In altri casi, come osservato negli studi sui ratti, un assone può avere origine da un dendrite. Alcuni assoni con origine dendritica hanno un segmento iniziale prossimale che inizia direttamente sull'origine dell'assone, mentre altri hanno un segmento iniziale distale, separato dall'origine dell'assone.[28] In molte specie alcuni neuroni hanno assoni che partono dal dendrite e non dal corpo cellulare.[29] In molti casi, l'assone ha origine sul soma. Alcuni assoni con origine somatica hanno un segmento iniziale prossimale adiacente al monticolo assonico, mentre altri hanno un segmento iniziale distale.[28]
Note
[modifica | modifica wikitesto]- ^ a b Alberts, Bruce., Essential cell biology, 2nd ed, Garland Science Pub, 2004, ISBN 081533480X, OCLC 52312215. URL consultato il 31 luglio 2018.
- ^ a b Alberts, Bruce,, Lewis, Julian, e Raff, Martin,, Molecular biology of the cell, 4th ed, Garland Science, 2002, ISBN 0815332181, OCLC 48122761. URL consultato il 31 luglio 2018.
- ^ Sadler, T. W. (Thomas W.), Langman's medical embryology., 11th ed., Lippincott William & Wilkins, 2010, ISBN 9780781790697, OCLC 227928523. URL consultato il 31 luglio 2018.
- ^ A. Hess e J. Z. Young, The nodes of Ranvier, in Proceedings of the Royal Society of London. Series B, Biological Sciences, vol. 140, n. 900, 20 novembre 1952, pp. 301-320. URL consultato il 31 luglio 2018.
- ^ a b c d Dominique Debanne, Emilie Campanac e Andrzej Bialowas, Axon Physiology, in Physiological Reviews, vol. 91, n. 2, 2011-04, pp. 555-602, DOI:10.1152/physrev.00048.2009. URL consultato il 30 luglio 2018.
- ^ Na Chen, Jiandong Yu e Hao Qian, Axons amplify somatic incomplete spikes into uniform amplitudes in mouse cortical pyramidal neurons, in PloS One, vol. 5, n. 7, 29 luglio 2010, pp. e11868, DOI:10.1371/journal.pone.0011868. URL consultato il 31 luglio 2018.
- ^ Wolpert, L. (Lewis),, Principles of development, Fifth edition, ISBN 9780198709886, OCLC 907379024. URL consultato il 30 luglio 2018.
- ^ T. L. Fletcher e G. A. Banker, The establishment of polarity by hippocampal neurons: the relationship between the stage of a cell's development in situ and its subsequent development in culture, in Developmental Biology, vol. 136, n. 2, 1989-12, pp. 446-454. URL consultato il 30 luglio 2018.
- ^ Hui Jiang e Yi Rao, Axon formation: fate versus growth, in Nature Neuroscience, vol. 8, n. 5, 2005-5, pp. 544-546, DOI:10.1038/nn0505-544. URL consultato il 30 luglio 2018.
- ^ K. Goslin e G. Banker, Experimental observations on the development of polarity by hippocampal neurons in culture, in The Journal of Cell Biology, vol. 108, n. 4, 1989-4, pp. 1507-1516. URL consultato il 30 luglio 2018.
- ^ Phillip Lamoureux, Gordon Ruthel e Robert E. Buxbaum, Mechanical tension can specify axonal fate in hippocampal neurons, in The Journal of Cell Biology, vol. 159, n. 3, 11 novembre 2002, pp. 499-508, DOI:10.1083/jcb.200207174. URL consultato il 30 luglio 2018.
- ^ A. J. Furley, S. B. Morton e D. Manalo, The axonal glycoprotein TAG-1 is an immunoglobulin superfamily member with neurite outgrowth-promoting activity, in Cell, vol. 61, n. 1, 6 aprile 1990, pp. 157-170. URL consultato il 30 luglio 2018.
- ^ Darío Kunik, Carolyne Dion e Tsuneyuki Ozaki, Laser-based single-axon transection for high-content axon injury and regeneration studies, in PloS One, vol. 6, n. 11, 2011, pp. e26832, DOI:10.1371/journal.pone.0026832. URL consultato il 30 luglio 2018.
- ^ Martin E. Schwab, Nogo and axon regeneration, in Current Opinion in Neurobiology, vol. 14, n. 1, 2004-2, pp. 118-124, DOI:10.1016/j.conb.2004.01.004. URL consultato il 30 luglio 2018.
- ^ Squire, Larry R., Fundamental neuroscience, 4th ed, Elsevier/Academic Press, 2013, ISBN 9780123858719, OCLC 830351091. URL consultato il 30 luglio 2018.
- ^ B. L. Andrew e N. J. Part, Properties of fast and slow motor units in hind limb and tail muscles of the rat, in Quarterly Journal of Experimental Physiology and Cognate Medical Sciences, vol. 57, n. 2, 1972-4, pp. 213-225. URL consultato il 30 luglio 2018.
- ^ N. J. Russell, Axonal conduction velocity changes following muscle tenotomy or deafferentation during development in the rat, in The Journal of Physiology, vol. 298, 1980-1, pp. 347-360. URL consultato il 30 luglio 2018.
- ^ Pocock, Gillian., Human physiology : the basis of medicine, 2nd ed, Oxford University Press, 2004, ISBN 0198585268, OCLC 53192607. URL consultato il 30 luglio 2018.
- ^ Eva-Maria Krämer-Albers, Katja Gehrig-Burger e Christoph Thiele, Perturbed interactions of mutant proteolipid protein/DM20 with cholesterol and lipid rafts in oligodendroglia: implications for dysmyelination in spastic paraplegia, in The Journal of Neuroscience: The Official Journal of the Society for Neuroscience, vol. 26, n. 45, 8 novembre 2006, pp. 11743-11752, DOI:10.1523/JNEUROSCI.3581-06.2006. URL consultato il 30 luglio 2018.
- ^ Reuben Matalon, Kimberlee Michals-Matalon e Sankar Surendran, Canavan disease: studies on the knockout mouse, in Advances in Experimental Medicine and Biology, vol. 576, 2006, pp. 77–93; discussion 361–363, DOI:10.1007/0-387-30172-0_6. URL consultato il 30 luglio 2018.
- ^ (EN) Dmitri Tkachev, Michael L. Mimmack e Stephen J. Huffaker, Further evidence for altered myelin biosynthesis and glutamatergic dysfunction in schizophrenia, in The International Journal of Neuropsychopharmacology, vol. 10, n. 04, 12 febbraio 2007, p. 557, DOI:10.1017/s1461145706007334. URL consultato il 30 luglio 2018.
- ^ Medcyclopaedia - Brain injury, traumatic, in archive.is, 26 maggio 2011. URL consultato il 30 luglio 2018 (archiviato dall'url originale il 26 maggio 2011).
- ^ Traumatic Brain Injury (TBI) - Definition, Epidemiology, Pathophysiology: Overview, Epidemiology, Primary Injury, 18 agosto 2017. URL consultato il 30 luglio 2018.
- ^ Finger, Stanley., Origins of neuroscience : a history of explorations into brain function, Oxford University Press, 1994, ISBN 0195065034, OCLC 27151391. URL consultato il 30 luglio 2018.
- ^ (EN) Jennifer L. Hellier, The Brain, the Nervous System, and Their Diseases [3 volumes], ABC-CLIO, 16 dicembre 2014, ISBN 9781610693387. URL consultato il 30 luglio 2018.
- ^ K. Hsu e S. Terakawa, Fenestration in the myelin sheath of nerve fibers of the shrimp: a novel node of excitation for saltatory conduction, in Journal of Neurobiology, vol. 30, n. 3, 1996-7, pp. 397-409, DOI:10.1002/(SICI)1097-4695(199607)30:3<397::AID-NEU8>3.0.CO;2-#. URL consultato il 30 luglio 2018.
- ^ J.L. Salzer e B. Zalc, Myelination, in Current Biology, vol. 26, n. 20, 2016-10, pp. R971–R975, DOI:10.1016/j.cub.2016.07.074. URL consultato il 30 luglio 2018.
- ^ a b Felix Höfflin, Alexander Jack e Christian Riedel, Heterogeneity of the Axon Initial Segment in Interneurons and Pyramidal Cells of Rodent Visual Cortex, in Frontiers in Cellular Neuroscience, vol. 11, 2017, p. 332, DOI:10.3389/fncel.2017.00332. URL consultato il 30 luglio 2018.
- ^ Lazaros C. Triarhou, Axons emanating from dendrites: phylogenetic repercussions with Cajalian hues, in Frontiers in Neuroanatomy, vol. 8, 2014, p. 133, DOI:10.3389/fnana.2014.00133. URL consultato il 30 luglio 2018.
Altri progetti
[modifica | modifica wikitesto] Wikizionario contiene il lemma di dizionario «assone»
Wikizionario contiene il lemma di dizionario «assone» Wikimedia Commons contiene immagini o altri file su assone
Wikimedia Commons contiene immagini o altri file su assone
Collegamenti esterni
[modifica | modifica wikitesto]- assone, in Dizionario di medicina, Istituto dell'Enciclopedia Italiana, 2010.
- (EN) axon, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | LCCN (EN) sh85010598 · GND (DE) 4200576-0 · J9U (EN, HE) 987007282443905171 |
|---|