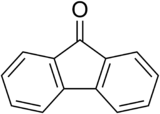
Fluorenone
| Fluorenone | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| 9-fluorenone | |
| Nomi alternativi | |
| 9H-9-fluorenone 9-ossofluorene difenilenchetone | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C13H8O |
| Massa molecolare (u) | 180,20202[1] |
| Aspetto | fiocchi gialli o polvere cristallina gialla |
| Numero CAS | |
| Numero EINECS | 207-630-7 |
| PubChem | 10241 |
| SMILES | C1=CC=C2C(=C1)C3=CC=CC=C3C2=O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,130[2] |
| Solubilità in acqua | non solubile in acqua |
| Temperatura di fusione | 83,5 °C |
| Temperatura di ebollizione | 342 °C |
| Indicazioni di sicurezza | |
| Punto di fiamma | 162 °C[3] |
| Frasi H | --- |
| Consigli P | --- [4] |
Il fluorenone è un composto organico aromatico avente formula molecolare C13H8O. È usato per produrre farmaci antimalaria.
Caratteristiche generali
[modifica | modifica wikitesto]Il fluorenone è un chetone policiclico a tre anelli, costituente dei combustibili fossili e prodotto di combustione incompleta. Ha un significante impatto ambientale (è una priorità per l'EPA), tuttavia alcuni batteri sono capaci di sfruttare il fluorenone come fonte di carbonio ed energia, trasformandolo in 9-fluorenolo.[1] Il fluorenone è insolubile in acqua, ma solubile in acetone ed etere etilico.
Usi e produzione
[modifica | modifica wikitesto]
Il fluorenone ha caratteristiche fluorescenti (emette nel violetto). Non è sintetizzato commercialmente, ma è ottenuto dalla frazione intermedia nel processo di produzione del catrame, in particolare dall'ossidazione del fluorene con ossigeno. Svolge un'importante funzione come catalizzatore metallocenico (come legante). È anche usato nella produzione di poliradicali per le resine.
Usati nella produzione di farmaci antimalaria, il fluorenone e i suoi derivati, hanno un ruolo significativo anche come materiale di base per coloranti e vernici. Essi sono dotati di funzioni utili come la sensibilità alla luce ed alla temperatura, resistenza al calore, conducibilità, resistenza alla corrosione e nell'individuazione di gruppi amminici. Per questo sono usati in misuratori termici o di luce, nella chimica dei cristalli liquidi, nella chimica della luminescenza, nella analisi spettrofotometrica e nella chimica dei complessi organo-metallici.
Indicazioni di sicurezza
[modifica | modifica wikitesto]Il fluorenone è un sospetto cancerogeno. Gli studi sugli animali hanno riscontrato, in alcuni casi, lo sviluppo di tumori sottocutanei. Tuttavia, i caratteri tossicologici di questo composto sull'uomo, non sono ancora stati totalmente studiati. Può causare irritazioni agli occhi, alla pelle, al tratto digestivo e respiratorio. Il fluorene è stabile a temperatura e pressione ambiente, ma è incompatibile con forti agenti ossidanti, può decomporre in monossido di carbonio ed anidride carbonica.
Interventi di primo soccorso
[modifica | modifica wikitesto]- Contatto con occhi: sciacquare abbondantemente con acqua per almeno 15 minuti. Consultare un medico.
- Contatto con la pelle: lavare abbondantemente con acqua e sapone. Rimuovere gli indumenti contaminati, da lavare prima di riusarli.
- Ingestione: se la vittima è cosciente e in allerta, ingerire 3-4 tazze di latte o acqua. Ma non somministrare nulla di orale ad una persona incosciente. Chiamare un medico.
- Inalazione: allontanare la vittima e portarla in un luogo aerato. Se non respira, fornire una respirazione artificiale, od ossigeno se la respirazione è difficoltosa. Chiamare un medico.
Misure antincendio
[modifica | modifica wikitesto]Come in ogni incendio, indossare un'attrezzatura adatta. Durante l'incendio si potrebbero sviluppare gas altamente tossici o irritanti dovuti alla combustione od alla decomposizione del composto. Metodi di estinzione adatti: acqua vaporizzata, polveri, anidride carbonica o schiuma.
Indicazioni di protezione
[modifica | modifica wikitesto]Indossare occhiali protettivi, guanti, camice e respiratore (per grandi quantità di fluorene).
Norme generali protettive e di igiene
[modifica | modifica wikitesto]Maneggiare e provvedere alla aerazione, minimizzare la produzione di polvere ed il suo accumulo nell'ambiente. Evitare il contatto con gli occhi, con la pelle e con gli indumenti. Mantenere i contenitori ermeticamente chiusi ed evitare ingestione ed inalazione.
Dispersione accidentale
[modifica | modifica wikitesto]Usare le protezioni adatte, come indicato sopra. Contenere le fuoriuscite immediatamente, osservando le giuste precauzioni. Raccogliere il composto e stoccarlo in contenitori adatti. Provvedere alla ventilazione del locale.
Smaltimento e stoccaggio
[modifica | modifica wikitesto]Tenere i contenitori chiusi, quando sono inutilizzati. Stoccare in ambiente fresco, asciutto e ben aerato, lontano da sostanze incompatibili con il fluorene. Gli ambienti in cui viene utilizzato o stoccato dovrebbero essere provvisti di doccia di sicurezza e lavandino per lavaggio degli occhi.
Sono state proposti tre metodi per lo smaltimento del fluorenone, due dei quali comprendono il metabolismo del composto da parte di batteri. Un batterio è capace di crescere sul fluorene, ma il metodo deve essere ancora studiato.[1] È supposto che il 9-fluorenone può essere trasformato in 9-fluorenolo tramite deidrogenasi, che può essere indotta nel batterio durante il suo sviluppo.[1]
Immagini 3D della molecola
[modifica | modifica wikitesto]

Note
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su fluorenone
Wikimedia Commons contiene immagini o altri file su fluorenone
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) Material Safety Data Sheet, su fscimage.fishersci.com.
- (EN) HSDB - Security Data Sheet on Fluorenone, su toxnet.nlm.nih.gov.
- (EN) NCBI Fluorenone's Summary, su pubchem.ncbi.nlm.nih.gov.
- (EN) Fluorenone's Specific Sheet, su chemicalland21.com. URL consultato il 16 marzo 2010 (archiviato dall'url originale il 2 aprile 2010).








