
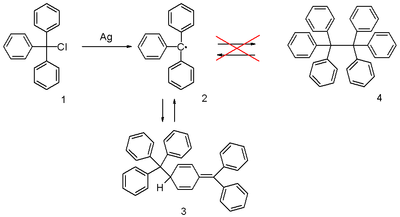
Il radicale trifenilmetile è un radicale persistente, ed è il primo radicale in assoluto ad essere stato descritto in chimica organica. Si può preparare per omolisi del cloruro di trifenilmetile 1 (Schema 1) con un metallo come argento o zinco in benzene o etere dietilico. Il radicale 2 è in equilibrio con il dimero in forma chinonica 3. In benzene la concentrazione del radicale è del 2%.[1]
Soluzioni contenenti il radicale sono gialle; al crescere della temperatura la colorazione gialla diventa più intensa perché l'equilibrio si sposta a favore del radicale in base al principio di Le Châtelier. All'inverso il colore sbiadisce se la soluzione è raffreddata.
Se esposto all'aria il radicale si ossida rapidamente formando il perossido (Schema 2) e la soluzione diventa incolore. Il radicale reagisce con lo iodio formando lo ioduro di trifenilmetile.

Il radicale fu preparato per la prima volta da Moses Gomberg nel 1900.[2][3][4] Egli tentò di preparare esafeniletano a partire da cloruro di trifenilmetile e zinco in benzene usando una reazione di Wurtz, e trovò che il prodotto era molto più reattivo del previsto, dato il suo comportamento con ossigeno e iodio.
La corretta struttura chinonica del dimero era stata suggerita sin dal 1904, ma questa struttura fu poco dopo abbandonata dagli scienziati a favore del esafeniletano, struttura 4 nello schema 1.[5] La struttura chinonica 3 fu riscoperta solo nel 1968, quando ricercatori della Vrije Universiteit di Amsterdam pubblicarono i dati 1H RMN.[6]
Note
[modifica | modifica wikitesto]- ^ J. March, Advanced Organic Chemistry, John Wiley & Sons, 1985, ISBN 0-471-88841-9.
- ^ M. Gomberg, An instance of trivalent carbon: triphenylmethyl, in J. Am. Chem. Soc., vol. 22, n. 11, 1900, pp. 757-771, DOI:10.1021/ja02049a006. URL consultato il 21 dicembre 2010.
- ^ M. Gomberg, On trivalent carbon, in J. Am. Chem. Soc., vol. 23, n. 7, 1901, pp. 496-502, DOI:10.1021/ja02033a015. URL consultato il 21 dicembre 2010.
- ^ M. Gomberg, On trivalent carbon, in J. Am. Chem. Soc., vol. 24, n. 7, 1902, pp. 597–628, DOI:10.1021/ja02021a001. URL consultato il 21 dicembre 2010.
- ^ J. M. McBride, The hexaphenylethane riddle, in Tetrahedron, vol. 30, n. 14, 1974, pp. 2009–2022, DOI:10.1016/S0040-4020(01)97332-6. URL consultato il 21 dicembre 2010.
- ^ H. Lankamp, W. Th. Nauta e C. MacLean, A new interpretation of the monomer-dimer equilibrium of triphenylmethyl- and alkylsubstituted-diphenyl methyl-radicals in solution, in Tetrahedron Letters, vol. 9, n. 2, 1968, pp. 249–254, DOI:10.1016/S0040-4039(00)75598-5. URL consultato il 21 dicembre 2010.
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su Radicale trifenilmetile
Wikimedia Commons contiene immagini o altri file su Radicale trifenilmetile
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) Molecola del mese, giugno 1997, su chm.bris.ac.uk. URL consultato il 22 dicembre 2010.
- (EN) Il radicale trifenilmetile: proprietà e sintesi (con dettagli sperimentali), su faidherbe.org. URL consultato il 22 dicembre 2010.








